Актин, тропонин, тропомиозин - основные сократительные белки мышц

Общие сведения
Мышечное волокно содержит маленькие субъединицы. Мышечое воловно содержит в себе от нескольких сотен до пару тысяч миофибрилл, - это сократительные элементы скелетной мышцы.
Из саркомеров, имеющих вид длинных нитей состоят миофибриллы. В каждой миофибрилле тесно друг с другом располагается около 3000 актиновых и 1500 миозиновых филаментов.
Актином образованы тонкие филаменты, более толстые - миозином. Молекула миозина состоит из двух сплетенных протеиновых пучков, а конец каждого пучка образует миозиновую головку.
Каждый филамент обладает рядом подобных головок, которые выходят вперед формируя поперечные мостики. Они взаимодействуют во время мышечного сокращения с активными участками на актиновых филаментах.
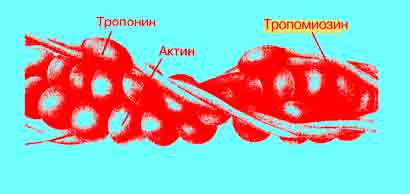
Рис. Актиновый, тропониновый и тропомиозиновый комплекс.
Актиновый филамент состоит из трех молекул:
- Актина
- Тропомиозина
- Тропонина.
На рисуноке 1 показан актиновый филамент, состящий из молекул актина, тропомиозина и тропонина.
Актиновые молекулы соединяясь вместе, образуют нити актиновых молекул. Соединяются нити, обвившись одна вокруг дрогой, в виде спирали вкрученные вместе.
Тропомиозин - один из основных, составляющих регуляторного аппарата, тонких филаментов во всех типах мышц. Молекулы тропомиозина - вытянутые, переплетаясь с семью мономерами актина и тропониновым комплексом в составе тонкого филамента. Тропонин представляет собой комплекс состоящий из трех белков:
- тропонин С, способного обратимо связывать ионы Са2+,
- тропонин I, который самостоятельно может ингибировать сокращение,
- тропонин Т,который взаимодействует с тропонинами I и С, а также прочно связывается с ТМ.
Открытие тропомиозина было - Bailey в 1946 г. С помощью электронного микроскопа было доказано, что тропомиозин образует длинные фибриллы, примерно схожего диаметра, которые деполимеризуются при повышении ионной силы раствора.
Молекулы тропомиозина, в состоянии покоя, распологаются над активными участками актиновых филаментов, предотвращая "привязывание" миозиновых головок. Тропомиозин совместно с тропонином принимают участие в регуляции актина с взаимодействием миозина. На концах каждой молекулы тропомиозина расположены белки тропониновой системы, наличие которой характерно только для поперечно-полосатых мышц. Не простая работа тропомиозина и ионов кальция нацелена на обеспечение сохранение состояния расслабления, либо формирование сокращения миофибриллы.
Ионы Ca2+ , в последствии выхождения из саркоплазматического ретикулума, вступают взаимосвязь с тропонином на актиновых филаментах. Тропонин, который имеет достаточно большое сходство к ионам кальция, приступает к процессу сокращения, "поднимая" молекулы тропомиозина с активных участков актиновых филаментов. ТМ зачастую "скрывает" активные участки, тем самым блокируя связь поперечных мостиков миозина с актиновым филаментом. Когда Ca2+ и тропонин "подымают" тропомиозин с активных участков, головки миозина начинают прикрепляться к активным участкам актиновых филаментов. При увеличении концентрации ионов кальция, в цитозоле мышечной клетки, запускается сокращение мышц, в ответ на внешние стимулы (иннервация, химическая стимуляция).
Лишь только тогда завершается мышечное сокращение, когда C2+ активно выкачивается из саркоплазмы назад в СР для хранения. Тропонин и тропомиозин инактивируются при удалении Ca2+, чем самым происходит разрыв связи поперечных мостиков миозина с актиновыми филаментами и прекращается использование АТФ. Филаменты, актина и миозина вследствие этого приходят в свое первоначальное расслабленное состояние.
Список литературы
- Уилмор Дж.Х., Костилл Д.Л., - Физиология спорта. Киев: / «Олимпийская литература», 2001г.
- Волков Н.И., Несен Э.Н., Осипенко А.А., Корсун С.Н.,- Биохимия мышечной деятельности / «Олимпийская литература», 2000 г
- Невзоров И. А., Левицкий Д. И. Тропомиозин: двойная спираль из мира белков // Успехи биологической химии. — Т. 51. — МАИК "Наука/Interperiodika" Пущино, 2011.
^Наверх









