Азол – производные азола (триазол, тетразол, имидазол, оксазол)

Азолы – 5-членные гетероароматические субстанции, которые содержат в цикле не менее 2 гетероатомов, один из которых является - атом азота, и поли- и бициклические конденсированные системы на основе азольного цикла. К этой группе соединений относятся моноциклические системы и их бензопроизводные: диазолы - пиразол (I), имидазол (II) триазол - 1,2,3 и 1,2,4-триазол (III и IV), тетразол (V), тиазол (VI), изотиазол (VII), оксазол (VIII), изоксазол (IX), окса- и тиадиазол (1,2,3, 1,2,4, 1,2,5-, 1,3,4-оксадиазол и тиадиазол, Х = О, S, X-XIII), индазол (бензопиразол) (XIV ) бензимидазол (XV), бензотиазол (XVI), 1,2-бензизотиазол (XVII), 1,2-бензизоксазола (XVIII), 2,1-бензизотиазол (XIX), 2,1-бензизоксазола (ХХ), бензотриазол ( ХХ):
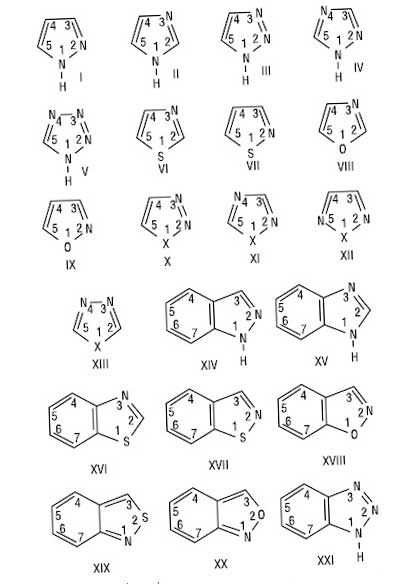
Для азолов применяют номенклатуру, которая объединяет систематические и тривиальные названия (Ганча - Видмана), однако, практически все наименования азотсодержащих соединений имеют в своем названии окончание «-азол». В молекулах диазолов, триазолов и тетразолов присутствуют два типа атомов азота в sp2-гибридизации: один - с парой электронов на р-АО ортогональной плоскости молекулы (кислотный центр), а второй - с парой электронов на sp2-АO в плоскости цикла (основной, нуклеофильный центр). Имидазол - основа средней силы, другие азолы - слабые основания; сила основы уменьшается с увеличением количества атомов азота в молекуле (-I-эффект). Добавки азолов менее основные, особенно если гетероатом находится рядом с центром протонирования. Кислотность азолов возрастает с увеличением количества атомов азота: триазол по кислотности можно сравнить с фенолом, а 1Н-тетразол - с ацетатной кислотой. N-незамещенный азол легко образуют водородные связи в жидкостных и твердых фазах. Формирования водородных связей менее вероятно в ряду N-замещенных азолов, оксазолов и триазолов. Для N-незамещенного ди-, три- и тетразол характерна прототропна таутомерия. Благодаря быстрому протонному переносу 3- и 5-замещеные пиразолы или 4- и 5-замещеные имидазолы взаимопревращаются настолько быстро, что их практически невозможно изолировать в чистом виде.
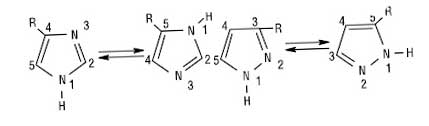
Таутомеры также могут существовать в растворах как правило в одной из форм. Азосоединения устойчивы к воздействию окислителей и кислот. Относительно к электрофильным агентам азосоединения менее активны, чем их пятичленные аналоги с 1 гетероатомом. Имидазол - амфотерное соединение. Катион имидазолила и имидазолил-анион - симметричные делокализованных структуры. Электрофильное замещения в сильнокислой среде блокируется протонированием атома азота, протекает преимущественно по положению 4 нуклеофильного замещения ориентированное по положению 2. В пиразол реакции SE проходят по положению 4. Для трех- и тетразолэлектрофильного замещение по атому углерода чуждо. Нуклеофильное замещение по сравнению с диазоламом протекает достаточно легко. Трех-, тетразол, содержащие группировки -N = N-, могут при нагревании или под действием света расщепляться с потерей азота. Оксазолы вступают в реакции присоединения и циклоприсоединения, а также проявляют слабый ароматический характер. В оксазоле, тиазоле и их бензоаналогах нуклеофильное замещение протекает по положению 2. В изоксазоле раскрытие цикла происходит слабой связью N-O, используют в синтетических целях. У некоторых оксадиазолов, тиадиазолов нуклеофильное замещение протекает быстро по положению, активированными атомами азота.
Имидазол входит в структуру аминокислоты гистидина и метаболита ее декарбоксилирования - гистамина. Гистидин остатки обнаружены в активных положениях рибонуклеазы и других ферментов. Производные имидазола широко используются в фармакологии: азомицин (2 нитроимидазол) - натуральный антибиотик, метронидазол - противомикробный препарат, клотримазол, бифоназол - антимикотические лекарственные средства. Имидазольный цикл включают в своем составе ряд циклических уреидов (гидантоин, парабановая кислота). Пиразол и его производные входят в состав лекарственных препаратов: аминофеназона амидопирина, метамизола натрия, фенилбутазона, которые оказывают противовоспалительное, анальгетическое и жаропонижающее действие. Тетразол играет важнейшую роль в медицинской химии, поскольку N-незамещённый тетразол можно считать аналогами карбоновых кислот. Синтетическим путем были получены аналоги природных карбоновых кислот и аминокислот, в молекулах которых карбоксигруппа замещена нететразольным циклом. Бензимидазол содержится в составе структуры витамина В12 некоторых фунгицидов, противоязвенных препаратов (в частности омепразола) и других лекарственных средств. Производные тиазола, в отличие от оксазола, имеют широкое распространение в природе: витамин В1 (тиамин), блеомицин антибиотики, которые оказывают противоопухолевую активность. Некоторые полусинтетические β-лактамы (цефотаксим) содержат фрагменты 2-аминотиазола в боковой цепи. Существует несколько природных изоксазолов, которые проявляют ценные фармакологические свойства. Мусцимол, выделенный из мухомора, оказывает сильное психотропное действие, влияет на нервные клетки мозга, которые используют γ-аминомасляную кислоту как нейротрансмиттер. Структура этой субстанции была взята за основу при производстве ряда синтетических изоксазолов как потенциальных анальгетических веществ. Циклосерин и изоксазолин - противотуберкулезные и противоопухолевые природные антибиотики. Некоторые полусинтетические пенициллины (оксациллин, клоксацилин, доклоксацилин) также содержат изоксазольний фрагмент в боковых цепях. Производные азолов также применяют в промышленном синтезе лекарственных препаратов, пестицидов, красителей, оптических отбеливателей и тому подобное.
^Наверх








