Синтез мочевины (орнитиновый цикл синтеза мочевины в гепатоцитах): Физиология, Патофизиология, Биохимия, Клиничское значение
Введение
Печень катаболизирует (превращает) токсический аммиак в мочевину в орнитиновом цикле, как показано на рисунке 1. Этот энергозависимый процесс происходит только в пределах митохондрий и цитоплазмы печени. Когда этот процесс не работает эффективно, токсический аммиак (NH3) накапливается в организме и может вызвать клинические проявления, такие как вялость, невнятная речь, отек головного мозга и астериксис.
Физиология: Цикл Мочевины
Здесь мы рассмотрим лежащую в основе физиологию цикла мочевины.
Ход протекания цикла синтеза мочевины
Цикл мочевины начинается в митохондриях гепатоцитов и заканчивается в цитоплазме. Следующие реакции будут показаны схематически под каждым описанным шагом. Обратите внимание, что фермент, ответственный за каждый соответствующий шаг, не будет показан, но его можно найти в предыдущем тексте.
Шаг 1
Первая стадия, которая также ограничивает скорость, включает преобразование СО2 и аммиака в карбамоилфосфат с помощью фермента карбамоилфосфатсинтетазы I (CPS I). Аммиак является источником первой аминной группы мочевины. Уникальность этого этапа заключается в том, что CPS I требует облигатного активатора, N-ацетил-глутамата (NAG). NAG возникает от глутамата + ацетил-КоА через фермент NAG-синтазу, которая может быть активирована аргинином. Следует отметить, что некоторые источники могут использовать NH и HCO+ в качестве исходных реагентов, но они эквивалентны CO2+ H2O + NH3.
CO2+ NH3+ 2 АТФ+H2O---карбамоилфосфат
Синтез NAG: глутамат + ацетил-КoA NAG
Шаг 2
Карбамоилфосфат и орнитин соединяются с образованием цитруллина через орнитин-транскарбамоилазу (OTC). Цитруллин после этого транспортирован от митохондрий гепатоцита в цитоплазму орнитин транслоказой.
Карбамоилфосфат + орнитин---цитруллин
Цитруллин в митохондриях---цитруллин в цитоплазме
Шаг 3
Цитруллин реагирует с аспартатом(аспарагиновая кислота) с образованием аргининосукцината. Эта реакция осуществляется ферментом аргининосукцинатсинтетазой, для которой требуется АТФ. Аспартат является источником второй аминной группы по мочевине. Напомним, что аспартат образуется в результате переаминирования оксалоацетата и глутамата через аспартаттрансаминазу, для чего необходим витамин В6.
Цитруллин + аспартат + АТФ---Аргининосукцинат
Оксалоацетат + глутамат(Глутаминовая кислота)---аспартат + Альфа-кетоглутарат
Шаг 4
Аргининосукцинат преобразуется в аргинин через аргининосукцинатную лиазу. Эта реакция также дает фумарат, который включается в митохондриальное образование НАДH в цикле ЦТК так же, как катаболизме тирозина.
Аргининосукцинат---аргинин + фумарат
Шаг 5
Аргинин подвергается гидролизу через аргиназу с образованием мочевины и орнитина. Уделите некоторое время рассмотрению шага 2. Обратите внимание, что регенерация орнитина в шаге 5 участвует в шаге 2.
Аргинин + H2O---мочевина + орнитин
Задействованные Системы Органов
Печень является единственным местом, где мочевина синтезируется и в конечном итоге выводится почками.
Функция
Цикл мочевины - это способ преобразования организмом токсичного аммиака в мочевину. Аммиак является следствием катаболизма протеина независимо от того, является ли он вторичным по отношению к высокобелковой диете, дезаминированию или в период длительного голодания. Аммиак также естественным образом вырабатывается кишечной микрофлорой. В мышцах и периферических тканях глутамат является той аминокислотой, которая принимает свободный аммиак, что приводит к образованию глутамина.
Глутамин после этого экспортируется от мышцы и периферийных тканей и используется печенью. Глутаминаза расщепляет глутамин на глутамат и аммиак. Глутамат также производит дополнительную мочевину через через фермент глутаматдегидрогеназу. Отсюда аммиак первоначально включается в митохондрии гепатоцитов и в конечном итоге приводит к образованию мочевины. Мочевина впоследствии выходит из цитоплазмы гепатоцитов и в конечном итоге выводится с мочой.
Связанное тестирование
Азот мочевины крови (АМК) - это обычно заказываемый тест, который измеряет уровень мочевины, обнаруженной в крови, и может оценить, насколько хорошо функционируют почки. Этот диапазон может незначительно отличаться в разных медицинских учреждениях, но АМК обычно составляет от 8 до 20 мг/дл. У пациентов с дисфункцией почек или высокобелковой диетой можно ожидать, что АМК будет повышена. Можно ожидать, что у пациентов с заболеванием печени или с нарушением цикла мочевины АМК будет уменьшен. Важно принять к сведению клиническую картину пациента, прежде чем предположить, что у пациента может быть почечная или печеночная дисфункция.
Сывороточный аммиак также может быть измерен и использован для оценки функционирования печени. Нормальный сывороточный аммиак обычно колеблется от 15 до 45 м / дл. Уровень аммиака в сыворотке крови может быть повышен у пациента с дисфункцией печени, нарушением цикла мочевины, избыточным ростом кишечной микрофлоры, катаболизмом белка и многими другими причинами. Опять же, важно оценить клиническую картину пациента, чтобы выявить причину повышенного содержания аммиака в сыворотке крови.
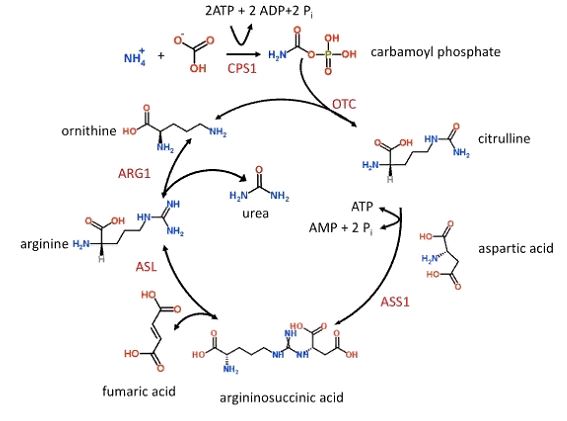
Рисунок 1. Ход протекания цикла синтеза мочевины
Патофизиология орнитинового цикла мочевины
Существует шесть клинически значимых расстройств. Поскольку все шесть из этих расстройств приводят к увеличению аммиака и снижению мочевины в крови, у каждого из них одинаковая клиническая картина. Гипераммонемия токсична для головного мозга и приводит к энцефалопатии, которая может проявляться отеком головного мозга, рвотой, помутнением зрения, астериксисом и судорогами. Избыток аммиака также приведет к повышенному образованию глутамина. Напомним, что глютаминсинтетаза использует реагенты NH3 и глутамат для получения глютамина. Глутамат является возбуждающим нейромедиатором, и поэтому снижение уровня глутамата вызовет подавленную нервную активность, которая проявляется в виде летаргии или коматозного состояния. Кроме того, избыток аммиака препятствует циклу ЦТК, вызывая образование Альфа-кетоглутарата глутамата.
Здесь мы обсудим наиболее распространенные нарушения цикла мочевины.
Дефицит орнитин-Транскарбамилазы (OTC)
Дефицит орнитинтранскарбамилазы является единственным Х-сцепленным рецессивным дефицитом фермента в цикле мочевины. Это также самый распространенный дефицит ферментов в цикле мочевины. Он приводит к повышению уровня карбамоилфосфата, который становится шунтированным в путь синтеза пиримидина, как только карбамоилфосфат попадает в цитоплазму. Карбамоилфосфат превращается в оротовую кислоту. Напомним, что оротовая кислота является предшественником всех пиримидинов. В результате этот дефицит приведет к повышению уровня оротовой кислоты в крови и моче. Оротическая ацидурия может проявляться в виде оранжевых кристаллов в подгузниках.
Дефицит Аргининосукцинатсинтетазы
Это расстройство является вторым наиболее распространенным дефицитом ферментов в цикле мочевины и является аутосомно-рецессивным. Из-за этого у пациентов будет повышен уровень цитруллина.
Дефицит Карбамоилфосфатсинтетазы I (CPS I)
Это расстройство также является аутосомно-рецессивным, но не приводит к повышению уровня оротовой кислоты. Дефицит CPS I часто приводит к летальному исходу в младенчестве.
При подозрении на дефицит фермента цикла мочевины ключ к выявлению источника проблемы основан на накоплении метаболитов. Например, дефицит OTC и дефицит CPS I приводят к снижению мочевины и повышенному аммиаку; однако дефицит OTC будет иметь повышенные уровни оротовой кислоты, тогда как дефицит CPS I не будет. Другой пример, дефицит OTC, и наследственная оротовая ацидурия оба имеют повышенную оротовую кислоту сыворотке крови и мочи. Одно различие между этими двумя состояниями вне их соответствующих ферментных дефицитов заключается в том, что дефицит OTC будет иметь повышенный уровень аммиака, в то время как наследственная оротическая ацидурия не будет.
Клиническое значение цикла синтеза мочевины
Понимая биохимические пути цикла мочевины, медицинские работники могут развивать свои знания и клинический подход в распознавании источника повышенного содержания аммиака и пониженного содержания мочевины у пациентов с возможным дефицитом ферментов цикла мочевины. При раннем выявлении дефицита цикла мочевины, пациенты, которые часто являются новорожденными и младенцами, могут быть “спасены” от возможных неврологических последствий. У пациентов с предполагаемым дефицитом мочевинного цикла дефицит орнитинтранскарбамилазы и дефицит аргининсукцинат-синтетазы должны быть в верхней части дифференциальных диагнозов.
Литература по физиологии и патологии цикла синтеза мочевины
- Kim D, Ko JM, Kim YM, Seo GH, Kim GH, Lee BH, Yoo HW. Low prevalence of argininosuccinate lyase deficiency among inherited urea cycle disorders in Korea. J. Hum. Genet. 2018 Jul;63(8):911-917.
- Moretto J, Girard C, Demougeot C. The role of arginase in aging: A systematic review. Exp. Gerontol. 2019 Feb;116:54-73
- Häberle J, Chakrapani A, Ah Mew N, Longo N. Hyperammonaemia in classic organic acidaemias: a review of the literature and two case histories. Orphanet J Rare Dis. 2018 Dec 06;13(1):219.
- Zhu S, Dong Z, Ke X, Hou J, Zhao E, Zhang K, Wang F, Yang L, Xiang Z, Cui H. The roles of sirtuins family in cell metabolism during tumor development. Semin. Cancer Biol. 2019 Aug;57:59-71.
- Adams S, Che D, Qin G, Farouk MH, Hailong J, Rui H. Novel Biosynthesis, Metabolism and Physiological Functions of L-Homoarginine. Curr. Protein Pept. Sci. 2019;20(2):184-193.
- Herrera PM, Vélez Van Meerbeke A, Bonnot O. Psychiatric Disorders Secondary to Neurometabolic Disorders. Rev Colomb Psiquiatr. 2018 Oct - Dec;47(4):244-251.
- Wang FS, Goh DLM, Ong HT. Urea cycle disorder presenting as bilateral mesial temporal sclerosis - an unusual cause of seizures: a case report and review of the literature. J Med Case Rep. 2018 Jul 15;12(1):208.
- Keshet R, Szlosarek P, Carracedo A, Erez A. Rewiring urea cycle metabolism in cancer to support anabolism. Nat. Rev. Cancer. 2018 Oct;18(10):634-645.
- Wild KT, Ganetzky RD, Yudkoff M, Ierardi-Curto L. Hyperornithinemia, Hyperammonemia, and Homocitrullinuria Syndrome Causing Severe Neonatal Hyperammonemia. JIMD Rep. 2019;44:103-107.
^Наверх









