Эффективность препаратов ингибиторов АПФ (ИАПФ) в терапии пациентов больных ХСН
Эффективность препаратов ИАПФ с начала их применения в клинической практике связывалась с их способностью влиять на нейрогуморальные механизмы регуляции и в первую очередь подавлять образование ангиотензина II, который представляет собой основной эффектор РААС. Так в исследовании CONSENSUS снижение риска смерти при использовании эналаприла в лечении больных ХСН было высокодостоверным и составило 40 % через шесть и 31 % через год лечения. При этом положительный эффект эналаприла сопровождался достоверным снижением содержания основных нейрогормонов в плазме крови по сравнению с группой контроля – ангиотензина II, альдостерона, предсердных натрийуретических факторов (ПНУФ), норадреналина.
Подтверждением высокой эффективности ингибиторов ИАПФ в лечении декомпенсации сердца (ХСН) являются результаты длительного наблюдения за больными, участвовавшими в конце 80-х годов в исследовании CONSENSUS. После очевидного выявления эффективности лечения эналаприлом и окончания двойной слепой фазы исследования, все пациенты были переведены на открытую терапию ИАПФ. Но и через два года, и через десять лет наблюдения сохранялась достоверная разница в прогнозе больных в зависимости от того, были ли они в первые 6-12 мес. на лечении эналаприлом или плацебо. Через десять лет в живых остались 5 из 127 больных, получавших ингибиторы АПФ и ни одного из группы плацебо. При этом необходимо учитывать, что исходно все больные имели крайне тяжелый III-IV ФК сердечной недостаточности. Определено, что эналаприл в 1,5 раза удлинял среднее время жизни больных - с 521 до 781 дня.
Однако несмотря на неоспоримые доказательства эффективности ИАПФ, в конце 80-х годов впервые сообщалось о возможности "ускользания" нейрогуморальных эффектов ИАПФ. Сначала это касалось содержания альдостерона. Было показано, что концентрация альдостерона в плазме крови максимально снижается на 40 % через две недели лечения каптоприлом, через восемь недель терапии степень его снижения уменьшается до 26 %, а через год терапии - до 13 % от исходного уровня, что недостоверно. В последующем отмечено, что влияние ИАПФ на формирование ангиотензина II также непостоянно и ослабевает со временем, как и влияние ИАПФ на ремоделирование сердца.
Приведенные данные явились предпосылками для концепции о неполной блокаде нейрогуморальных систем сердца у больных с ХСН при длительном применении ИАПФ и предложения комбинировать ингибиторы АПФ с другими нейрогуморальными модуляторами. Так в связи с наличием альтернативных (не АПФ-зависимых) путей образования ангиотензина II, не контролируемых ИАПФ, для полной блокады РААС возможно применение АРАII.
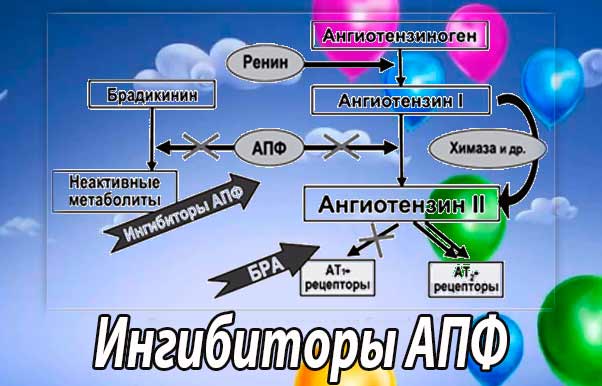
В норме около 75 % ангиотензина II образуется не-АПФ – зависимым путем при помощи химазы и некоторых других ферментов. Однако у больных ХСН ведущая роль в патогенезе принадлежит ангиотензинпревращающему ферменту, который относится к группе ферментов металлопротеаз, активным центром АПФ являются ионы цинка. При кратковременной терапии ИАПФ ингибируется АПФ-зависимый путь синтеза ангиотенрина II и, следовательно, его эффекты, направленные в том числе и на продукцию альдостерона. Однако при длительном применении ингибиторов АПФ постепенно активируется не АПФ-зависимый путь продукции ангиотензина II с частичным восстановлением его эффектов. Указанный механизм и может являться причиной “ускользания” части нейрогуморальных эффектов ИАПФ при длительной терапии больных с ХСН. Очевидно, что АРАII, действующие на уровне рецепторов, не уменьшат степень воздействия на РААС, что важно при длительном лечении сердечной декомпенсации.
Препараты ИАПФ список:
- эналаприл
- каптоприл
- рамиприл
- лизиноприл
- фозиноприл
- квинаприл
- спираприл
Толерантность к ингибиторам иАПФ также рассматривается как потенциальный камень преткновения для их использования, возможно самым значительным примером которой является вызываемый ИАПФ сухой кашель, возникающий вследствие замедления метаболизма брадикинина.









